Destruction de la rouille par électrolyse |
La rouille
Tout d'abords, il est bon de noter que l'état naturel du fer est l'état oxydé. Le fer métallique est obtenu par un traitement du minerai rouge contenant des oxydes de fer dans les hauts fourneaux, il tend à retourner à l'état oxydé lorsqu'il est exposé à l'air et à l'eau puisqu'il s'agit de sa forme naturel.La rouille est donc le résultat de l'oxydation du fer lorsqu'il est en présence de dioxygène et d'eau par le biais de phénomènes chimiques appelés oxydoréduction. La rouille est une structure cristalline complexe composée principalement d'oxydes de fer mais aussi d'hydroxydes de fer.
Voici de l'équation bilan très simplifiée de formation de la rouille
4Fe + 3O2 + 6H2O → 4Fe3+ + 12OH– → 4Fe(OH)3 → 2Fe2O3 . 3H2O
Dans les différents processus rentrant dans cette équation on retrouve la réduction du dioxygène de l'air dissous dans l'eau :
⇒ O2 + 2H2O + 4e– → 4OH–
Ainsi que l'oxydation du fer :
⇒ Fe + 2OH– → Fe(OH)2 + 2e–
On voit ainsi que l'eau et l'air sont nécessaire à l'apparition de la rouille. Une solution saline (eau de mer, route salée humide,…) favorise les déplacements ioniques de réaction d'oxydoréduction et donc augmente la vitesse de formation de la rouille.
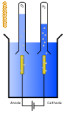 Il est heureusement possible de créer une autre réaction d'oxydoréduction afin de détruire cette rouille en créant des ions H+ autour de la pièce métallique par électrolyse de l'eau :
Il est heureusement possible de créer une autre réaction d'oxydoréduction afin de détruire cette rouille en créant des ions H+ autour de la pièce métallique par électrolyse de l'eau :2H2O (liquide) → 2H2 (gazeux) + O2 (gazeux)
Ces ions H+ vont s'allier aux ions O– contenus dans l'oxyde de fer Fe2O3 et faire disparaitre la rouille.
Voilà pour la partie théorique qui ne parlera certainement pas à tout le monde… (J'ai galéré de mon coté à essayer de comprendre l'intégralité du processus de formation et de destruction de la rouille).
Réalisation de l'électrolyse

 Attention : ce procédé n'est pas sans danger!
Attention : ce procédé n'est pas sans danger!- Utilisation de courant électrique : toutes les précautions relatives à l'utilisation de courant électrique doivent être mises en œuvre
- Utilisation de soude : c'est un produit corrosif, il faut travailler avec des gants et des lunettes de protection
- Dégagement de dihydrogène : il faut travailler dans un local bien aérée voir même à l'extérieur si possible.
Attention bis : Tous les métaux n'apprécie pas l'électrolyse : les pièces en aluminium sont à éviter par exemple, surtout dans un bain de soude.
Matériel nécessaire :
- Un bac en plastique- Un morceau d'acier inoxydable pour réaliser l'anode
- De l'eau, de préférence de l'eau de pluie ou de l'eau déminéralisée, mais de l'eau du robinet convient bien
- De la soude (soude caustique en cristaux type Saint Marc ou débouche-canalisation Destop)
- Une source de courant 12V (chargeur de batterie ou alimentation PC : voir plus bas)
Mode opératoire :
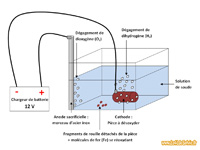 Remplir le bac avec de l'eau et y déposer l'anode métallique en acier inoxydable de manière à ce que celle-ci ne bouge pas. Brancher la borne + de la source de courant (qui n'est pas encore branché) sur ce morceau d'inox (Anode).
Remplir le bac avec de l'eau et y déposer l'anode métallique en acier inoxydable de manière à ce que celle-ci ne bouge pas. Brancher la borne + de la source de courant (qui n'est pas encore branché) sur ce morceau d'inox (Anode).Brancher la borne négative sur la pièce à dérouiller (cathode) et la plonger dans le bain électrolytique.
Attention : la pièce à dérouiller ne doit à aucun moment toucher l'anode en acier inox sinon cela créerait un court-circuit.
Attention : Ne pas inverser le sens des bornes sinon cela produirai l'effet inverse de l'effet souhaité et augmenterai significativement la corrosion de la pièce à désoxyder.
Brancher la source de courant et commencer à incorporer la soude dans l'eau. La soude à pour effet d'augmenter la conductivité de l'eau et donc d'augmenter le mouvement des électrons mais aussi, entre autre, de limiter la corrosion du métal (l'acier rouille moins facilement en milieu alcalin). Pour le dosage, il est un peu aléatoire et dépendra de la soude utilisée, de la quantité d'eau,...
Des bulles commencent à se former : dioxygène (O2) sur l'anode et dihydrogène (H2) sur la cathode. C'est les bulles de dihydrogène qui vont permettre à la fois le décollement de la rouille par frottement (action mécanique) et aussi sa réduction par phénomène d'oxydoréduction (action chimique)
Laisser agir quelques heures. Une fois toute la rouille réduite la pièce ne craint rien et peu rester dans le bain électrolytique pendant longtemps.
Après avoir tout débranché sortir la pièce et la brosser avec une brosse métallique. La pièce est de nouveau très vulnérable à l'oxydation, il faut alors rapidement la peindre ou la stocker convenablement afin d'empêcher celle-ci de s'oxyder de nouveau.
Remarques :
- L'anode ne doit pas obligatoirement être en acier inoxydable, ce peux être un morceau de fer a béton, mais celui-ci vas s'oxyder et devra être changé entre chaque électrolyse.
- Il n'est pas obligatoire d'utiliser la soude comme sel pour l'électrolyte, on peu très bien utiliser du sel de cuisine, cependant avec la soude l'électrolyse est plus efficace et possède d'autres avantages que je ne détaillerai pas ici car ils font encore intervenir des processus physico-chimique qui me dépasse.
La source de courant 12V :
Chargeur de batterie :
 Les nouveaux modèles de chargeur de batterie de bonne qualité "intelligent" ne fonctionne pas pour une électrolyse.
Les nouveaux modèles de chargeur de batterie de bonne qualité "intelligent" ne fonctionne pas pour une électrolyse.Il faut donc utiliser un chargeur bon marché.
J'en ai trouvé un chez Norauto à 15€, j'ai juste eu à remplacer le fusible de 5 Ampères qui à pété au bout de quelques minutes par un plus gros de 30A.
 J'utilise sinon un vieux chargeur de batterie qui n'est pas "intelligent" et qui ne s'encombre pas de fusible. Niveau sécurité ce n'est pas le meilleur mais il fonctionne à merveille et ce depuis des années.
J'utilise sinon un vieux chargeur de batterie qui n'est pas "intelligent" et qui ne s'encombre pas de fusible. Niveau sécurité ce n'est pas le meilleur mais il fonctionne à merveille et ce depuis des années.Alimentation de PC ATX :

 Il est aussi possible d'utiliser une alimentation de PC ATX en shuntant 2 bornes du connecteur ATX : la borne d'alimentation principale avec un fil vert et une borne de masse (fil noir) afin que le courant circule dans les prises Molex.
Il est aussi possible d'utiliser une alimentation de PC ATX en shuntant 2 bornes du connecteur ATX : la borne d'alimentation principale avec un fil vert et une borne de masse (fil noir) afin que le courant circule dans les prises Molex.Il ne reste alors plus qu'à se brancher sur une prise Molex : la borne positive +12V sur le fil jaune et la borne négative sur un des fils de masse noir. Le fil rouge de la prise Molex délivre quant à lui du +5V.
 Pour plus de détails sur l'utilisation d'une alimentation ATX comme source de courant ou sa transformation en alimentation d'atelier il suffit de jeter un œil à l'article dédié subtilement nommé Transformation d'une alimentation de PC en alimentation d'atelier.
Pour plus de détails sur l'utilisation d'une alimentation ATX comme source de courant ou sa transformation en alimentation d'atelier il suffit de jeter un œil à l'article dédié subtilement nommé Transformation d'une alimentation de PC en alimentation d'atelier.La mise en application sur des pièces de 4L
1er essai :
J'ai réalisé mon premier essai sur les 2 premières pièces particulièrement rouillées qui me sont tombées sous la main. Je ne les pas brossées, ni dégraissées, ni même enlevé la peinture qui restait. La source de courant est un chargeur mathusalemique appartenant à mes parents.Conclusion du 1er essai :
Après 3 heures d'électrolyse, le résultat est assez probant, même si le collier d'échappement est moins désoxydé que la poulie. Ceci est peut être du au fait que le collier était plus oxydé à la base et qu'il n'est pas fait dans le même alliage que la poulie. Ou peut être aurait il fallu le laisser plus longtemps.
La graisse qui restait sur la poulie à évidement gêné l'électrolyse (ça ne se voit pas très bien sur la photo mais il reste de la rouille aux quelques endroits ou l'épaisseur de graisse dépassait le mm), il est donc important de dégraisser convenablement la pièce avant l'électrolyse.
La peinture par contre n'a pas résisté longtemps et s'est décollée pendant le bain mais je ne sais pas si c'est du à l'électrolyse ou à la soude.
2ème essai :
Pour mon 2ème essai j'ai utilisé la même méthode que précédemment mais avec des pièces bien dégraissées. La source de courant est un chargeur de batterie "premier prix" (15€) acheté chez Norauto sur lequel j'ai changé le fusible de 5A qui avait tendance à péter trop rapidement pour un plus gros de 30A.Conclusion du 2ème essai :
Après environ 4 heures d'électrolyse, le résultat est parfait, la vieille peinture s'est décollée et toute la rouille est partie après un bon brossage à la brosse métallique.
3ème essai :
Toujours la même méthode avec des pièces bien dégraissées sauf que la source de courant change encore une fois : j'ai ce coup ci utilisé une alimentation de PC modifié comme décrit plus haut.Conclusion du 3ème essai :
Après environ 4 heures d'électrolyse, le résultat est parfait comme toujours. Il reste cependant de la peinture qui est bien accrochée mais si elle a résisté à la soude, à l'électrolyse et à la brosse métallique, je doit pouvoir repeindre par dessus sans aucun soucis.











